【炎症反応の説明できる?】炎症とサイトカインについて
老化したヘルパーT細胞の動き
なんと、「免疫の老化」と「個体の老化」は関連していた…!老齢マウスに「若い細胞移植」「古い細胞除去」でわかった驚愕の事実
2023.11.17 現代ビジネス
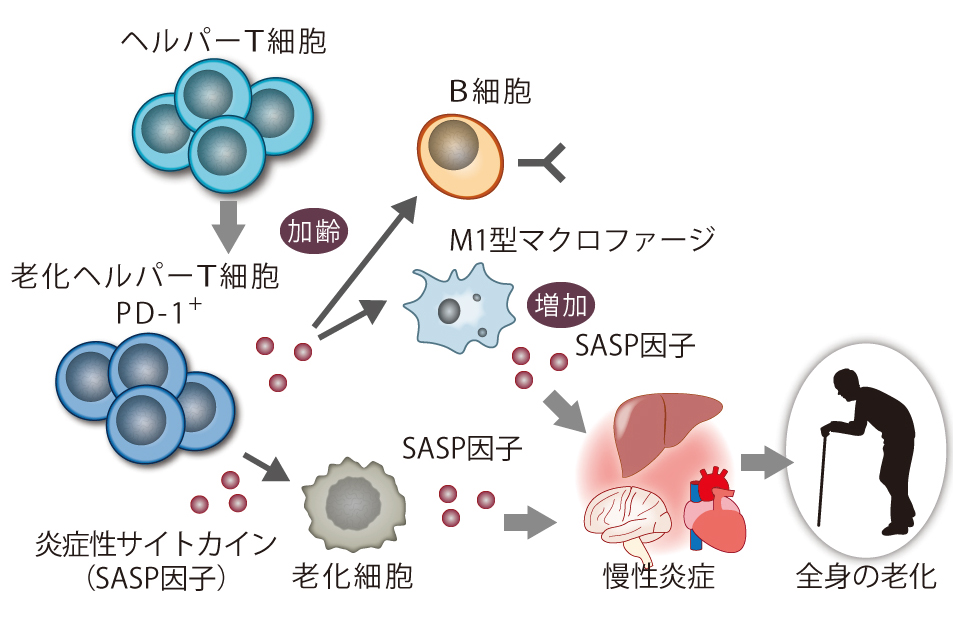
●老化したヘルパーT細胞の動き
老化ヘルパーT細胞は、ヘルパーとしての機能は低下するのですが、インターロイキン‐6(IL‐6)やオステオポンチンなど炎症性のサイトカインは余計に分泌します。
また、インターロイキン‐21(IL-21)も産生します。老化ヘルパーT細胞が分泌する炎症性物質は、老化細胞が分泌するSASP(細胞老化関連分泌形質)因子の仲間です。
こうして起きる免疫老化に付随すると考えられている慢性炎症は、心血管疾患、動脈硬化症、がん、糖尿病、慢性腎臓病、非アルコール性脂肪肝、自己免疫疾患や神経変性疾患などの老化関連疾患を促進することがわかってきました。このような加齢に伴う慢性炎症による老化の促進を「炎症老化(inflammaging)」と呼びます。
https://gendai.media/articles/-/119100?page=3
LIFESPAN(ライフスパン)―老いなき世界
【目次】
はじめに――いつまでも若々しくありたいという願い
■第1部 私たちは何を知っているのか(過去)
第1章 老化の唯一の原因――原初のサバイバル回路
第2章 弾き方を忘れたピアニスト
第3章 万人を蝕(むしば)む見えざる病気
■第2部 私たちは何を学びつつあるのか(現在)
第4章 あなたの長寿遺伝子を今すぐ働かせる方法
第5章 老化を治療する薬
第6章 若く健康な未来への躍進
第7章 医療におけるイノベーション
■第3部 私たちはどこへ行くのか(未来)
第8章 未来の世界はこうなる
第9章 私たちが築くべき未来
おわりに――世界を変える勇気をもとう
-
-
-
-
-
-
-
-
-
- -
-
-
-
-
-
-
-
-
第6章 若く健康な未来への躍進 より
未来の選択肢①老化細胞を除去する
老化の典型的特徴の1つが「老化細胞の蓄積」だったのを思い出してほしい。老化細胞とは、増殖するのを永久にやめてしまった細胞のことだ。
若いヒト細胞を培養すると、40~60回ほど分裂したところでテロメアが致命的な短さになる。この限界点は、発見者である解剖学者のレナード・ヘイフリックにちなんで「ヘイフリック限界」と呼ばれている。テロメラーゼという酵素があればテロメアを伸ばすことができるのだが(この発見によってエリザベス・ブラックバーン、キャロル・グレイダー、ジャック・ゾスタックの3人が2009年のノーベル賞を受賞した)、細胞ががん化するのを防ぐために、幹細胞以外ではこの酵素のスイッチが切られている。だが1997年、驚くべき事実が明らかになった。培養した皮膚細胞にテロメラーゼを注入すると、細胞が老化しないのである。
テロメアの短縮がなぜ老化を引き起こすかについては、ほぼ解明されている。テロメアが非常に短くなると、その部分ではヒストンへの巻きつきが緩み、まるで革紐の先の金具が取れたかのように染色体末端のDNAがむき出しになる。細胞はその状態をDNAが切断された結果だと判断する。だからDNAの末端を修復しようとするが、そのとき別々の染色体の末端同士を融合させてしまうことがある。こうなると、細胞分裂の際に染色体が引きちぎられたり再結合したりしてゲノムがきわめて不安定になり、それが繰り返されるうちに細胞ががん化するおそれが出てくるのだ。
テロメアが短くなったときには、もっと安全な解決策がある。細胞の機能を止めてしまうことだ。それは、サバイバル回路を働きっぱなしにさせる結果として起きると私は考えている。テロメアがむき出しになって、DNAが切断したとみなされると、サーチュインなどのエピゲノム調節酵素は本来の持ち場から駆り出されたままになる。しかし、修復しようにも、つなぐべきもう一方のDNA末端が見当たらない。結果的に細胞の複製能力は停止する。それはちょうど、高齢の酵母のDNAが損傷することでSir2(サーチュイン、SIR1からSIR7まである)が接合型遺伝子から離れ、生殖能力が失われるのとよく似ている。
DNAが損傷したときと同じ反応が生じ、エピゲノムに大きな変化がもたされる現象は、ヒトの老化細胞で実際に起きることが確認されている。ICEマウス(エピゲノムを変化させることで老化が進んだのと同じ状態にしたマウス)の細胞にエピゲノムの雑音を加えた場合も、通常の細胞より早く老化が進むことがわかっている。だとすれば、私の考え方には見るべきところがありそうだ。神経細胞や筋肉細胞(ほとんどないしまったく分裂しない)が老化するのは、エピゲノムの雑音が原因であり、そのせいで細胞は本来のアイデンティティを失って活動を停止するのではないか。私はそう思っている。この反応は、DNAを損傷しても細胞が生き残れるようにするために進化したものなので、もともとは有益なものだ。しかし、負の側面も併せもっている。細胞が絶え間ないパニック状態に陥り、辺りにシグナルを送って、周囲の細胞をもパニックに陥れるのだ。
老化細胞によるダメージのメカニズム
老化細胞はよく「ゾンビ細胞」と表現される。いっそ死んでくれればいいのに、死ぬのを拒んでいるからだ。薄い組織片を凍らせて特殊な染色剤を加えると、ゾンビ細胞のところだけが青色に染色されてくっきりと見える。これは、ゾンビ細胞がつくるβ-ガラクトシダーゼという珍しい酵素が染料と反応するためだ。組織の老化が進んでいるほど、青い細胞が増える。たとえば、20代の白色脂肪細胞は白いが、中年では淡い青に、老年では濃い青に染まる。ぞっとするではないか。老化細胞の数が多いとすれば、体が老化の魔手に落ちている証拠なのだ。
老化細胞はたとえ数が少なくても、広い範囲にダメージを及ぼしかねない。分裂をやめているとはいえ、サイトカインという小さなタンパク質を放出し続けて炎症を起こし、免疫細胞のマクロファージを引き寄せて組織を攻撃させるのだ。慢性的な炎症は体に良くない。多発性硬化症や炎症性腸疾患、あるいは乾癬にかかっている人に訊いてみたらわかるはずだ。こうした病気は、すべてサイトカインが多すぎるために引き起こされる。炎症はまた、心臓病、糖尿病、認知症の引き金にもなる。エイジング(老化)に伴う病気の発症にインフラメーション(炎症)が中心的な役割を果たすことから、科学者はそのプロセスをよく「インフラメイジング(炎症性老化)」と呼ぶ。しかも、サイトカインは炎症の原因になるだけではない。生物界の黙示録さながらに、ほかの細胞までをもゾンビ化させる。こうなると、さらに周囲の細胞を刺激してがん化させ、それが広がるおそれさえ出てくる。
マウスの老化細胞を破壊すると、マウスが格段に健康になってかなり長生きすることがすでにわかっている。腎臓が健全に機能する機関も長くなるうえ、心臓のストレス耐性も高まる。メイヨー・クリニックの研究では、結果としてマウスの寿命が20~30%延びるのが確認された。疾患モデル動物で老化細胞を除去すると、線維性肺疾患の肺は柔軟性を増し、緑内障や変形性関節症の進行が遅くなり、あらゆる種類の腫瘍が小さくなる。
なぜ生物は老化するようになったのか、それを理解するのは学術的な研究のためばかりではない。老化細胞を防いだり破壊したりするうえで、より良い方法を編み出す役に立ってくれるからだ。細胞が老化するのは、私たちが原初のサバイバル回路を受け継いだ結果である。サバイバル回路とは、DNAの損傷が感知されたときに細胞の分裂や生殖を止めるよう進化したものだ。DNAの切断があまりに頻繁に起きたり、サバイバル回路に対する負荷が大きすぎたりすると、ヒトの細胞は分裂をやめ、パニックに陥ったままダメージを修復しようとする。高齢の酵母細胞の場合とまったく同じだ。そのせいで自らのエピゲノムを乱し、サイトカインを分泌する。これが細胞老化の最終段階だ。お世辞にも有終の美とはいえない状態である。