食物繊維で免疫改善!クロストリジウムたちの働き 腸内空間メイキング 動画 YouTube
https://www.youtube.com/watch?v=kRD3n1gDtNI
A two module model of Treg function.
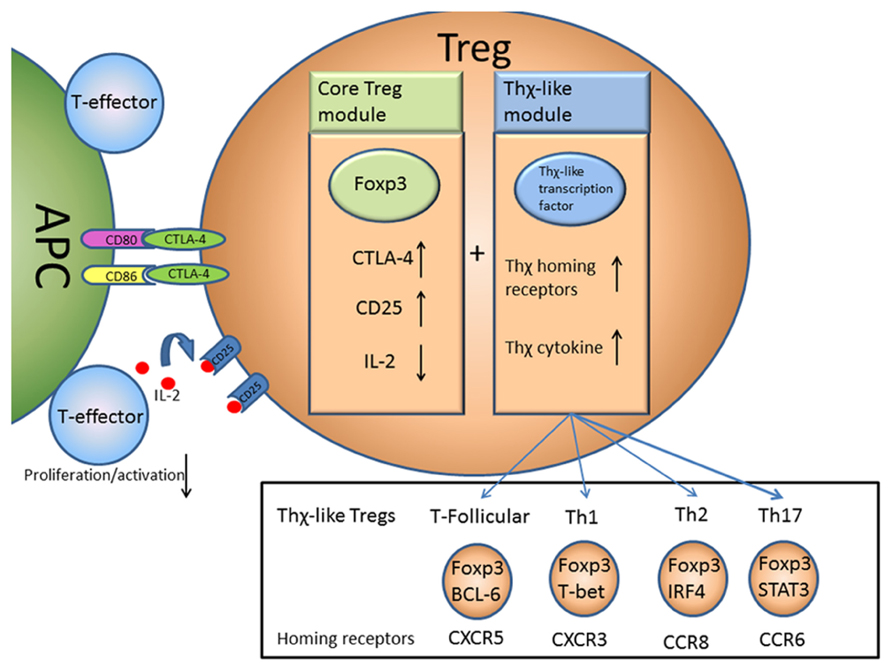
Multiple treg suppressive modules and their adaptability 29 June 2012 Frontiers
●James B. Wing and Shimon Sakaguchi
Foxp3+ regulatory T cells (Tregs) are a constitutively immunosuppressive cell type critical for the control of autoimmunity and inflammatory pathology.
https://www.frontiersin.org/articles/10.3389/fimmu.2012.00178/full
NHKスペシャル 「人体 神秘の巨大ネットワーク(4)万病撃退!腸が免疫の鍵」 2018年1月14日 健康ch
【司会】タモリ、山中伸弥、久保田祐佳 【ゲスト】田中将大、小島瑠璃子
ひとたび、腸で免疫のバランスが崩れ、免疫細胞が暴走を始めると大変なことに。
花粉や食べ物、自分の体の一部まで「敵」と誤って攻撃し、さまざまなアレルギーや免疫の病を引き起こしてしまう。どうすれば、腸内細菌が出す“メッセージ”を活用してこの暴走を抑え、アレルギーなどを根本解決できるのか。最先端の顕微鏡映像や高品質のCGを駆使して、知られざる腸の力に迫る。
腸に7割が集中するといわれる免疫細胞。
患者さんの腸内で減少していたクロストリジウム菌という腸内細菌は、腸の中で何をしているのでしょうか。その謎を解く鍵は、免疫研究の世界的権威、大阪大学特任教授の坂口志文さんが発見した「特別な免疫細胞」にありました。これまで免疫細胞と言えば、外敵を攻撃するのが役目と思われていましたが、坂口さんが新たに発見された免疫細胞は、その逆。むしろ仲間の免疫細胞の過剰な攻撃を抑える役割を持つことが突き止められました。その免疫細胞は、「Tレグ(制御性T細胞)」と名付けられています。免疫細胞の中には、「攻撃役」だけでなく、いわば「ブレーキ役」も存在していたのです。このTレグの働きで、全身の各所で過剰に活性化し暴走している免疫細胞がなだめられ、アレルギーや自己免疫疾患が抑えられていることがわかってきました。
なんとそんな大事なTレグが、腸内細菌の一種であるクロストリジウム菌の働きによって、私たちの腸でつくり出されていることが、最新研究で明らかになってきました。
https://www.nhk.or.jp/kenko/special/jintai/sp_6.html
『土と内臓 (微生物がつくる世界)』 デイビッド・モントゴメリー、アン・ビクレー/著、片岡夏実/訳 築地書館 2016年発行
体内の自然 より
共生生物の本当の重要性は、やはり数字を検討することで明らかになる。微生物の細菌の数が、特に腸内では、われわれ自身のものを大きく上回ることを思い出してほしい。そして細菌の重さは100万分の1グラムのそのまた100万分の1にすぎないが、人間のマイクロバイオームを全部合わせると数キログラムになる。ヒトの皮膚1平方インチに約50万個の微生物が棲んでいる――ワイオミング州の人口とほぼ同じだ。人間の体内には天の川の星の数よりたくさんの微生物がいる。私たち一人ひとりが微生物の銀河を持っているのだ。そして細菌の場合、ある人のマイクロバイオームを構成する微生物の組み合わせ全体は、指紋のように固有であるだけでなく、時とともに変わる。50歳になってからのマイクロバイオームは、2歳のときのマイクロバイオームと似ても似つかない。
・
カリフォルニア工科大学の微生物学者、サーキス・マズマニアンは、共生生物が炎症の調整を助けていることを示す説得力のある事例を集めているマイクロバイオーム研究者の一人だ。その研究グループの実験によって、腸に棲むバクテロイデス フラジリスがどのように免疫系と相互作用するかが解明されている。マウスを使った実験であるが、その結果は、ヒトの大腸内で見られるB・フラギリスなどの粘液に棲む細菌が、私たちの免疫反応にどう影響するかを示している。だが、マズマニアンの発見をくわしく検討する前に、発見当時の考え方を振り返ってみよう。
長い間、樹上細菌が提示できるのはタンパク質断片でできた抗原のみだと推測され、したがってT細胞受容体――キラーT細胞、Treg、TH17細胞に無数にあるすべて――はタンパク質断片にしか適合できないと考えられていた。なにしろ科学者が抗原を分析して見つかったのが、タンパク質断片だけだったのだ。だが、B・フラギリスは、そうでないことを証明したのだ。
・
だが、B・フラギリスは正確にはどのように大腸炎を治したのだろうか? マズマニアンらはそのメカニズムを見つけるために探求を続けた。すると、ポリサッカライドA(PSA)抗原を積載した樹状細胞は、抗炎症性のTregを活性化させることがわかったのだ! B・フラギリスは、どうやら、宿主であるマウスの体じゅうの平和を保ちながら、自分自身は免疫系の標的になることを避けているようだ。そうすることで、この細菌はすみかを確保しているのだ。これは全員が得をしているということだろうか?
もう一つの実験で、マズマニアンはB・フラギリスの抗炎症効果をきっちりと証明した。マズマニアンはB・フラギリスからPSAを抽出し、不純物を取り除いて、実験的に大腸炎にかからせたマウスに与えた。マウスに現れた効果は、B・フラギリスそのものを投与したのと同じだった。思ったとおり大腸炎は治り、マウスはすぐに回復した。
マズマニアンはさらに研究を行ない、B・フラギリスが誘導したTregについてさらに多くを知った。問題のTregは、インターロイキン10という炎症を抑えるサイトカインを分泌して、大腸炎を治すのだ。まだ大腸炎にかかっているマウスでは、別のT細胞とサイトカインがはたらいていた。大腸炎のマウスには、比較的高い数値でTH17細胞があり、これが炎症を誘導するインターロイキン17を作っていた。
B・フラギリスは消化管の場所に邸宅した場合に問題を起こすことがあるが、マズマニアンらの実験は、B・フラギリスが少なくともマウスの腸では病気を治す力を持つことを示している。
日本の研究者も、ヒトの大腸粘膜に棲む共生生物に関心を抱いていた。B・フラギリス以外の細菌もTregの発生に影響があるのか? いくつかの実験で彼らは、さまざまな共生生物について大腸炎にかかった無菌マウスを回復させる能力をテストした。このメカニズムは、Tregの発生を誘導することによって起きるという仮説を、彼らは立てた。彼らは驚くべき発見に行き当った――Treg発生の最大のブースターはただ1種類の細菌ではなかったのだ。それはクロストリジウムという細菌のグループに属する特定の17の菌株の組み合わせだった。